
المشاركة الأصلية كتبت بواسطة yahoo52
القانون الثانى من الديناميكا الحرارية يستخدم كثيرا فى قضية هل لهذا الكون اله ام لا لكن هذا ليس صحيح لان:
1- هو ليس قانون فيزيائى بالمعنى المحدد لكلمة قانون و الدليل اذكر لى الاثبات الرياضى له و معادلتة . انه احد الاستنتاجات المنطقية من قانون بقاء الطاقة (الذى هو احد القواعد الكلاسيكية ايضا)
|
بخصوص الأنتروبية
مصطلح إنتروبية entropy (يعرب أحيانا بكلمة اعتلاج ) مصطلح أساسي و مفصلي ضمن التحريك الحراري خاصة بالنسبة للقانون الثاني للترموديناميك ، الذي يتعامل مع العمليات الفيزيائية و يبحث في شروط كونها عملية تلقائية ام لا . ينص القانون الثاني على مبدأ أساسي يقول بأن تغير تلقائي في نظام فيزيائي لا بد و ان يترافق بازدياد في مقدار إنتروبية هذا النظام. تميل التغيرات التلقائية عموما لأن تعدل من الاختلافات في الحرارة ، الضغط ، الكثافة ، و أيضا الكمون الكيميائي ضمن أي نظام فيزيائي او كيميائي بحيث تقلل الفوارق لأقل مقدار ممكن ليصل النظام لحالة من التوازن . الإنتروبية ضمن هذا المفهوم هي مقدار تقدم عملية التعديل هذه . بالمقابل ، نجد القانون الأول في الترموديناميك يتعامل مع مصطلح الطاقة التي تكون عادة محفوظة ضمن نظام فيزيائي مغلق . في نفس الوقت تعرف الإنتروبية على أنها تغير نحو حالة أكثر فوضوية على المستوى الجزيئي فالتغيرات التلقائية تميل دوما لكسب مزيد من الحرية لحركة الجزيئات او الذرات . في السنوات الأخيرة ، بدأ التعبير و شرح الإنتروبية على أنها "تشتت" dispersal للطاقة. تعتبر الإنتروبية دالة حالة انتشارية extensive تصف و تقيم تأثيرات اللاعكوسية في النظمة الترموديناميكية .
و يرمز عادة ل الإنتروبية أو الاعتلاج بS أحد المصطلحات الأساسية في التحريك الحراري تمثل قياسا لمقدار الطاقة في النظام الفيزيائي التي لا يمكن استخدامها لإنتاج عمل ، و هذا يؤول بكلام آخر من منظور الميكانيك الإحصائي إلى أنها مقياس لمدى العشوائية أو انعدام النظام في الجملة الفيزيائية ، و يمكن على هذا الأساس القول أن الإعتلاج أيضا هو مقياس لمدى قابلية قلب عملية ترموديناميكية ما. في الترموديناميك تشكل الإنتروبية متغيرا فيزيائيا مهما لوصف نظام ترموديناميكي.
نظام الواحدات الدولي أقر أن وحدة الإنتروبية هي بالجول لكل كلفن (J·K?1) ، و هي نفس واحدة السعة الحرارية، حيث تعتبر الإنتروبية مرافقة conjugate لدرجة الحرارة .
سنة 1865 استعمل العالم رودولف كلاوسيوس مصطلح الإنتروبية و قدم التعريف التالي لها:
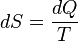
حيث T هي درجة الحرارة, Q مقدار الطاقة الحرارية و S مقدار الإعتلاج. و يمكن تحوير هذه المعادلة حتى تأخذ بعين الإعتبار قيمة العمل الضائع و ذلك عن طريق الإنطلاق من دالة لالجهد الترموديناميكي و بالتحديد من المعادلة للطاقة الداخلية:
U = U(S,V)
إذا قمنا بحساب التفاضل الكلي للطاقة الداخلية فإننا نتحصل على:

أي أن:

و إذا إستعنا بالصيغة التفاضلية للقانون الأول للتحريك الحراري:
dU = dQ ? pdV + dWdissp حيث dWdissp = هو العمل الضائع و على هذا الأساس يمكن كتابة المعادلة التي تعرف الإنتروبية بهذه الطريقة:

و عن طريق هذه المعادلة نرى أن قيمة الإنتروبية تزداد أو تنقص إذا قمنا بتزويد نظام ما بالطاقة الحرارية أو سحبها منه. كما أنه مع تزايد قيمة العمل الضائع تتزايد الإنتروبية (العمل الضائع دائما موجب). كما أنه يمكن أن نقرأ من هذه المعادلة أنه بالنسبة لنظام أدياباتي (أي لا يمكنه تبادل طاقة حرارية أو مادة مع المحيط) أو نظام مغلق (لا يتبادل طاقة حرارية و لا عمل مع المحيط) فإن الإنتروبية لا يمكنها إلا أن تزداد. حيث أنه مثلا لا يمكن لكوب معزول حراريا تحصل فيه عملية إختلاط غير قابلة للعكس بين سائلين إلا أن تزداد فيه الإنتروبية.
و تعتبر الإنتروبية متغير حر في الجهود الترمودينامية مثل الضغط و درجة الحرارة التي تصف الخواص المجهرية المقيسة للنظام .
يوجد ارتباط مهم بين الإنتروبية و مقدار الطاقة الداخلية في النظام التي لا يمكن تحويلها لعمل . ففي أي عملية عندما يعطي النظام طاقة بمقدار ?E ، و تنخفض إنتروبيته بمقدار ?S فإن مقدارا TR ?S من هذه الطاقة على الأقل يجب أن يذهب لمحيط النظام بشكل حرارة غير قابلة للاستعمال ، و إلا فإن العملية لن تستمر . (TR هي حرارة المحيط الخارجي للنظام، الذي لا يمكن ان يكون بنفس درجة حرارة النظام T ).
سنة 1865 اقترح لودفيغ بولتزمانوفق الميكانيك الإحصائي تعرقفا ىخر للإنتروبية. حسب بولتزمان تعتبر الإنتروبية مقياس لإحتمال حالة فزيائية معينة. و قد صاغ ذلك في القانون التالي:
S = k.lnW
حيث k هي ثابت بولتزمان و تساوي 1,380662.10 ? 23J / K و W هي احتمال حدوث حالة ترموديناميكية. و لفهم هذه المعادلة يمكننا تخيل نظام يتكون من جزيئين A و B و أن النظام يحتوي على 3 كوانتات من الطاقة فإن الحالة الترموديناميكية تتكون من موقع الجزيء في النظام و لنقل مثلا أنه هناك موقعين ممكنين مثلا كأن يكون الجزيء A في الموقع م1 و B في الموقع م2 أو العكس أي أن هناك إحتمالين لموقع الجزيئات ثم هناك أربع إحتمالات لتوزيع كوانتات الطاقة على الجزيئات ( مما يعطينا في المجموع ثمانية حالات ترموديناميكية للنظام و إذا إعتبرنا أن جميع الحالات لها نفس إحتمال الحدوث فإن قيمة الإنتروبية تعادل:
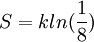
عامة يمكن إعتبار المعادلة التالية للإنتروبية:

حيث ?i هو الكمون الكميائي, p الضغط, T الحرارة, n عدد مولات مادة معينة في النظام. و انطلاقا من هذه المعادلة يمكن أن نرى أن الإنتروبية مهمة جدا لتعريف مصطلح التوازن الترمودينامي. حيث أنه في حالة التوازن الترمودينامي و التي هي الحالة التي يتوق و يحاول أي نظام أن يصل إليها نجد أن القوى الترمودينامية قد إختفت (المعاملات بين القوسين في المعادلة أعلاه) أي أن النظام له نفس الضغط كمحيطه و نفس درجة الحرارة و نفس الكمون الكميائي أو التركيز.
ولعل من المعادلات المهمة في سياق ذكر الأنتروبية ما يعرف بعلاقات ماكسويل:

و التي يمكن أن نستنتج منها عدة علاقات مثل:

و لا يزال علماء الفيزياء يقرون بصحة القانون الثاني للترموديناميك

2- قانون بقاء الطاقة بالمعنى الذى يفهمة معظم الناس خطا . و بالتالى القانون الثانى للديناميكا الحرارية خطا. هو يبدوا صواب على المنظور المرئى العادى لكن عند دراسة نظرية الكم سوف تكتشف انه يخضع لاحتمالات
3- الدليل على ذلك ان الفراغ المطلق تتكون فية جسيمات دون الحاجة لمصدر خارجى للطاقة ولكن هذة الجسيمات سرعان ما تفنى بحيث يصبح فى متوسط زمنى معين تكون مجمل الطاقة صفر . و هذا يناقض مبدا بقاء الطاقة . فوجود طافة او جسيمات فى فراغ مطلق يخضع للاحتمال فقط . انا اعرف ان هذا الكلام يبدو غير منطقى ولكنه حقيقة .فلا يوجد مكان خالى من الجسيمات . و كاما قلت المسافة وقصر الزمن ازداد احتمال تكون الجسيمات
|
الفضاء مليء بالطاقة وهذا معروف
و انتقال الطاقة و الجسيمات لا يعني استحداث الطاقة من عدم أو افناء الطاقة
و لا يزال العلماء يقرون بالقانون الأول للترموديناميك (قانون حفظ الطاقة)
نظرية الكم وضعها العلما لتفسير بعض الظواهر الفيزيائية التي لا يمكن تفسيرها بالنظريات الكلاسيكية فلذلك لا تصلح أن تكون نظرية عامة
إقرأ هذا المقال
http://www.makphys.com/vb3/showthread.php?t=807
حدود تطبيق النظريتين الكلاسيكية و الكمية
سوف أناقش في هذا التلخيص البسيط الذي قمت بكتابته مؤخرا متى يمكننا إستخدام النظريات الكلاسيكية و متى يمكننا إستخدام النظريات الكمية .
او متى يمكننا إستخدام النظريات في "الحدود النسبية" و "الحدود اللانسبية"
و اول سؤال يخطر في بالنا
هل هناك ثابت يمكننا على أساسه إستخدام النظريات المناسبة ؟
انه ثابت بلانك و يرمز له تقريبا بالرمز (h) و قيمته تساوي
h = 6.626 * 10^-27 erg sec
or h = 60626*10-34 joule sec
و على هذا فإن الأبعاد الفيزيائية لهذا الثابت هي
زمن * طاقه = طول * كمية تحرك خطي = كمية تحرك زاوي
و يطلق على هذه الكمية الفيزيائية مصطلح الفعل (action) و بالتبيعة فإن ثابت بلانك يسمى كم الفعل الأساسي .
إذا بعد ان تعرفنا قليلا على ثابت بلانك
سوف نستعرض متى يمكنا إستخدام كلا من النظريتين الكلاسيكيه و الكمية
بالنظر لمتغير الغعل الذي يمثل أي حالة فيزيائية
زمن * طاقه = طول * كمية تحرك خطي = كمية تحرك زاوي
إذا كان نظام فيزيائي متغير ديناميكي أي اننا يمكننا تمييز حالة النظام مثل إحداثيات الموقع , مركبة كمية التحرك ...... الخ و كان له قيمة عددية مقاربه لثابت بلانك فإن عمل هذا النظام يجب ان يوصف في إطار ميكانيكا الكم
أما إذا كان للمتغير قيمة عددية كبيره جدا مقارنة بثابت بلانك فقوانين الفيزياء الكلاسيكة تكون صالحه لدرجة كافيه للتطبيق .
مثال للتوضيح ...
لنفترض متذبذا توافقيا صغيرا لكنه عياني ,,,, و لتكن كتلته 1 gm و سرعته العظمى 1 cm / sec و سعته العظمى
x = 1 cm لذا سوف تكون كمية تحركه العظمى p = 1 gm cm sec^-1
و الكمية xp = 1 erg sec هي متغير الفعل للمتذبذب التوافقي
نلاحظ من انه مقارنة بثابت بلانك h = 6.626 * 10^-27 erg sec ان القيمة كبيره جدا و لذلك لا يمكننا تطبيق النظريات الكمية ... و يمكن معالجتها كلاسيكيا ..
فكلما كان متغير الفعل قريبا من ثابت لانك كلما امكننا تطبيق النظريات الكمية ...
و للحديث بقيه في مواضيع أخرى متنوعة
المرجع :
مقرر بيركلي في الفيزياء(الفيزياء الكمية)
 4- دعك من فكرة نظرية الكم الصعبة هناك مثال واحد اخر يمكن ان يفند القانون الثانى للدينياميكا الحرارية دون الحاجة لنقض قانون بقاء الطاقة :
4- دعك من فكرة نظرية الكم الصعبة هناك مثال واحد اخر يمكن ان يفند القانون الثانى للدينياميكا الحرارية دون الحاجة لنقض قانون بقاء الطاقة :
اذا افترضنا ان الكون به كتلة تزيد عن الكتلة الحرجة(الكتلة اللازمة لوقف تمدد الكون و اعادة انجذابة نحو مركز واحد مرة ثانية) فهذا يعنى ان الكون ككل نظام ليس له انتروبيا (سوف يكون هناك تبادل حرارى وانتروبيا لكل مكون من مكوناتة فيما بينها لكن الكون ككل وكنظام واحد لن يكون له انتروبيا ) وبذلك سوف يرتد الكون نحو مركز واحد ثم ينفجر ثانية وهكذا دون ان يضطر للرجوع الى السكون
ملحوظة :الكون الذى نعيش فية يبدو ان كتلتة اقل من الكتلة الحرجة وانه سيتمد الى ما لا نهاية .
|
قد يتمدد الكون الى نقطة معينة ثم يبدأ بالتقلص وهكذا دواليك هذا كلا من الحيث المبدأ مقبول علميا ولكن ليس إلى اللأنهاية فكل مرة من تمدده وتقلصه تكون الأنتروبية قد ازدادت وحتى تصل إلى قيمتها العظمى وعندها تنعدم كل العمليات التلقائية للجملة (الكون هنا) و تنعدم معها الحياة
فتمدد الكون و تقلصه لا ينفي السكون الأنتروبي
http://www.astro.ucla.edu/~wright/cosmology_faq.html
The final entropy of the Universe as it approaches the Big Crunch singularity would be larger than the initial entropy of the Universe because of the heat added by nuclear fusion in stars, so a recollapse does not involve a decrease in entropy
the oscillating universe could not be reconciled with the second law of thermodynamics : entropy would build up from oscillation to oscillation and cause heat death
أي أن في كل دورة من التقلص و التمدد المفترضة تزداد فيه الأنتروبية و لن تعود النتروبية إلى مستوها السابق عند التقلص المفترض
السكون و الحركة أمر نسبي حسب المراقب و الجملة المقارنة
و السكون الأنتروبي مصطلح علمي و في السكون الأنتروبي تنعدم الأفعال التلقائية ولا تنعدم الحركة ففي تجربة مزج غازين وبعد تمام الإمتزاج لا تتوقف حركة الغازين وإنما تصبح نسبتهما في كلا الوعائين واحدة
وكذلك عند انتقال الحرارة من الجسم الساخن إلى الجسم البارد فتستمر بإنتقال حتى تتساوى درجة حرارة الجسمين وعندها يتوقف انتقال الحرارة ولكن لاتتوقف حركة الجسمين فالذرات و الجزيئات و الإلكترونات في حركة مستمرة قبل التوازن و بعده
 5- انت افترضت ان العلماء يفترضوا ان للكون ليس له بداية و لذلك ينبغى ان يكون دخل الى حالة السكون منذ زمن بعيد
5- انت افترضت ان العلماء يفترضوا ان للكون ليس له بداية و لذلك ينبغى ان يكون دخل الى حالة السكون منذ زمن بعيد
لكن هذا ليس صحيح فهناك العديد من النظريات التى تفترض بداية للكون و اصل للمادة ورغم انها كلها نظريات غير موكدة لكن غير قابلة للتكذيب ايضا وهى كلها تعتمد على فكرة تكون المادة فى الفراغ المطلق(الذى هو نظرية اساسية فى ميكانيكا الكم التى هى احد ركيزتين للفيزياء الحديثة ) ، او تعتمد ان هناك كون اخر تفرعنا منه عن طريق ثقوب دودية (وههذا استنتاجات من نظرية النسبية التى هى الركيزة الثانية للفيزياء الحديثة) و بما اننا لسنا فى الكون الثانى فاننا سوف يصعب علينا حاليا معرفة اصل كوننا سو ف تقول لوكان كذلك لتكونت اكوان اخرى و كنا سوف نلاحظها
اقول لك لا يوجد دليل انه لم تتكون اكوان اخرى وسالة ملاحظتها فالفضاء لانهائى و سرعة نقل المعلومات فية للتتجاوز سرعة الضوء (طبقا للنسبية الخاصة) و بالتالى قد يكون هناك عدد لانهائى من الجرات فى الفضاء اللانهائى
او حتى قد يكون الذى نراه هو اتحاد لعدة اكوان اخرى
|
معظم العلماء كانو يقولون بثبات الكون و لكن هذه النظرية لم تعد تلاقي الترحيب في الوسط العلمي بعد نشوء نظرية الأنفجار العظيم أو الكبير إلا أن علماء الفيزياء الملحدين يقولون بأزلية المادة و في هذا المقال تم دحض هذه المقولة
نظرية الكم كما ذكرت سابقا لم تستطيع خرق مبدأ حفظ الطاقة و المادة و لكن عمليات التحول من مادة إلى طاقة و بالعكس فهذا ممكن و هذا ما ذكرته في المقال
و جود كون آخر أو عدة أكوان أولا لا دليل عليه ثانيا لا يغير من الأمر شيء فيمكن إعتبار كل هذه الأكوان في جملة واحدة و بالتالي تكون مغلقة لأن الماديين لا يعترفون بأي شي خارج حدود المادة و هذا يعطينا نفس النتيجة جملة مغلقة و إزدياد في الأنتروبية و سكون مطلق لكل الأكوان المفترضة و بالتلي سكون أنتروبي للكون الذي نعيس فيه
السكون الأنتروبي حتمية لا بد منها بعد فترة من ظهور المادة أيا كان شكلها
 وانا اعرف ان هذا الراى الذى تقوله يويدة عدد من علماء الفيزياء قليل نسبيا . وهناك عدد اكبر يومن بالراى الذى القيت الضوء على بعض النقط فية . لكن غالبية العلماء يرو اننا نحتاج لمزيد من المعرفة عن الكون و الاهم عن مكونات هذا العالم (فمثلا نحتاج لنظرية لتوحيد القوى و وصفها وصفا دقيقا ونريد تفسير للمادة المظلمة) قبل ان نستطيع ان نقول راى عن اصل هذا الكون وانا مع الراى الاخير
وانا اعرف ان هذا الراى الذى تقوله يويدة عدد من علماء الفيزياء قليل نسبيا . وهناك عدد اكبر يومن بالراى الذى القيت الضوء على بعض النقط فية . لكن غالبية العلماء يرو اننا نحتاج لمزيد من المعرفة عن الكون و الاهم عن مكونات هذا العالم (فمثلا نحتاج لنظرية لتوحيد القوى و وصفها وصفا دقيقا ونريد تفسير للمادة المظلمة) قبل ان نستطيع ان نقول راى عن اصل هذا الكون وانا مع الراى الاخير
|
أنا لا أناقش كيف بدأ الكون و كيف سيحصل بالفعل في نهاية الكون
ولكن أناقش نهاية الكون بإفتراض أن المادة أزلية وبالنقاش تبين أنه لا يمكن للمادة أن تكون أزلية
نهاية المادة بالسكون الأنتروبي غير صحيحة لانها لو كانت صحيحة لوصلت المادة منذ زمن بعيد إلى السكون الأنتروبي
فهذا دليل واضح على أن المادة ليست أزلية
المجموعة كبيرة من الاراء العلمية في علم الكون والفيزياء الكونية والتي تتحدث عن احتمالات مختلفة ومتباينة حول مصير الكون
هي تدعم رأيي و تدعم مقالي وهي تنفي السكون الأنتروبي للكون و بالتالي الكون كله و المادة كله مخلوقة وليست أزلية
 و اتمنى ان يكون الرد دون هجوم شخصى وان يكون النقاش حول راى علمى
و اتمنى ان يكون الرد دون هجوم شخصى وان يكون النقاش حول راى علمى
|
نحن في منتدى علمي و لم أشعر بأن ردك هو هجوم شخصي و مشكور أخي على جراءتك
و أهلا بك صديقا عزيزا
بالمناسبة قمت بمناقشة هذا الموضوع "هل لهذا الكون من إله" في منتدى ملحد و كذلك قمت بمناقشة موضوع انخفاض درجة حرارة الكون إذا كنت مهتم بالأمر أو أي أحد مهتم بالأمر فيمكنني تلخيص ما دار من نقاش و وضعه في المنتدى