أهلا وسهلا بك إلى ملتقى الفيزيائيين العرب.
أهلا وسهلا بك زائرنا الكريم، إذا كانت هذه زيارتك الأولى للمنتدى، فيرجى التكرم بزيارة صفحة التعليمـــات، بالضغط هنا.
كما يشرفنا أن تقوم بالتسجيل بالضغط هنا إذا رغبت بالمشاركة في المنتدى، أما إذا رغبت بقراءة المواضيع والإطلاع فتفضل بزيارة القسم الذي ترغب أدناه.
| ملتقى الفيزيائيين العرب > قسم المناهج الدراسية > فيزياء المرحلة الثانوية. > الصف الثالث الثانوي | ||
| سلسلة المُساعد(45 - 50): شرح ومناقشة " الفيزياء النووية " | ||
| الملاحظات |
|
|
أدوات الموضوع | انواع عرض الموضوع |
|
#1
|
|||
|
|||
|
سلسلة المُساعد(45 - 50): شرح ومناقشة " الفيزياء النووية "
بسم الله الرحمن الرحيم
أخوتي الكرام ، السلام عليكم ورحمة الله وبركاته ، وبعد : بين أيديكم الدروس من 45 إلى 50 من سلسلة المُساعد ، والتي تتطرق إلى : " فصل : الفيزياء النووية " للإطلاع على الفصول السابقة ، تفضل عبر الروابط التالية : سلسلة المُساعد( 1 - 13): " الكهربــائيـــة" سلسلة المُساعد( 14-24 ): " المغناطيسية" سلسلة المُساعد(25- 34): " الإلكترونيات " سلسلة المُساعد(35- 44): " الذريـــــــــة "[/ خريطة معرفـيّة لفصل "الكهربائيّــة" ( ربط جميع مفردات الفصل الثامن ) خريطة ذهنيـّة بالصور لفصل المغناطيسيّة ( ربط جميع مفردات الفصل التاسع ) خريطة معرفـيّة لفصل "المغناطيســــيّة" ( ربط جميع مفردات الفصل التاسع ) اللهم علمنا ما ينفعنا وانفعنا بما علمتنا وزدنا علما يا رب العالمين . لا تنسوني ووالديّ وأهلي من صالح دعائكم في ظهر الغيب . |
|
#2
|
|||
|
|||
|
الفيزياء النووية: تهتم الفيزياء النووية بدراسة نوى العناصر من حيث تركيبها و خواصها و تفاعلاتها ، وللتفاعلات النووية أهمية خاصة في إنتاج الطاقة أو استهلاك الطاقة . ومن المعلوم أن النواة تحتوي على بروتونات ونيوترونات حيث أن : البروتونات : جسيمات موجبة الشحنة يرمز لها بالرمز ( P ) وكتلة البروتون الواحد 1.00727663 و.ك.ذ . النيوترونات: جسيمات غير مشحونة ( متعادلة الشحنة ) يرمز لها بالرمز ( n ) وكتلة النيوترون الواحد 1.0086654 و.ك.ذ . 1 و.ك.ذ = 1.6604 × 10 ^-27 كجم و لكل عنصر عدد ذري يكتب يسار رمز العنصر من الأسفل وعدد كتلي يكتب يسار رمز العنصر من الأعلى كالتالي :  العدد الذري (A ) = عدد البروتونات العدد الكتلي (Z ) = عدد البروتونات + عدد النيوترونات |
|
#3
|
|||
|
|||
|
التحولات ( التغيرات ) الطبيعية التي تحدث للنواة : [flash=http://www.phys4arab.net/uploood/naser/nuclear01.swf]WIDTH=700 HEIGHT=400[/flash] http://www.phys4arab.net/uploood/naser/nuclear01.swf أولاً : إشعاع ألفـ(α)ـــا He : - تعريفه : هو عبارة عن تيار من جسيمات موجبة الشحنة ( أثقل من الإلكترون بحوالي 7000 مرة تقريباً ) استطاع رذرفورد أن يحرفه عن مساره باستخدام مجال مغناطيسي . - صفات جسيمات ألفا : 1) نفاذيتها خلال المواد ضعيفة حيث يمكن إيقاف إشعاع ألفا وامتصاصها بسهولة باستخدام صفيحة رقيقه من الألمنيوم لا يتعدى سمكها 0.05 ملم . 2) تؤين ذرات الهواء عند مروره . 3) أنها عبارة عن أيونات غاز الهليوم ( He++ ) أي تحتوي على بروتونين ونيوترونين . - كيفية إنتاج جسيمات ألفا :تنبعث غالباً من النويات ذات العدد الكتلي الكبير مثل اليورانيوم 238 و نواة الراديوم . - المعادلة الأساسية لها : 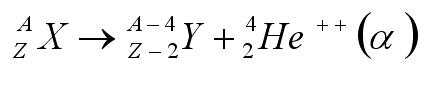 [flash=http://www.phys4arab.net/uploood/naser/nuclear02.swf]WIDTH=500 HEIGHT=100[/flash] http://www.phys4arab.net/uploood/naser/nuclear02.swf - التغير الحاصل في الذرة عند إصدار جسيم ألفا : ينقص العدد الكتلي 4 وحدات وينقص العدد الذري وحدتين . |
|
#4
|
|||
|
|||
|
ثانياً : أشعاع بيتا الســ(β)ــالبة( – e): - تعريفه : هو عبارة عن جسيمات ( شحنات ) سالبة تسمى الإلكترونات . - صفات جسيمات بيتا السالبة : نفاذيتها عالية فقدرتها أكبر 100 مرة من قدرة نفاذ جسيمات ألفا حيث تحتاج إلى صفيحة من الألمنيوم سمكها 5 ملم لإيقاف معظمها . - كيفية إنتاج جسيمات بيتا السالبة : تتولد في النويات غير المستقرة والتي تكون فيها نسبة النيوترونات أكبر من البروتونات ولذلك يتحول النيوترون إلى بروتون وإلكترون هذا الإلكترون يمثل جسيمات بيتا السالبة - المعادلة الأساسية لها : 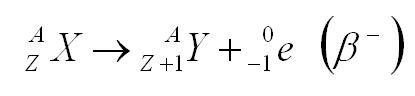 [flash=http://www.phys4arab.net/uploood/naser/nuclear03.swf]WIDTH=500 HEIGHT=100[/flash] http://www.phys4arab.net/uploood/naser/nuclear03.swf [flash=http://www.phys4arab.net/uploood/naser/nuclear12.swf]WIDTH=500 HEIGHT=400[/flash] http://www.phys4arab.net/uploood/naser/nuclear12.swf - مثال : الثوريوم 234 و البروتاكتينوم 234 . - التغير الحاصل في الذرة عند إصدار جسيم بيتا السالب : 1) العدد الذري يزيد وحدة ( أي يزيد بروتون واحد ) أما العدد الكتلي ثابت . 2) يتحول العنصر إلى عنصر آخر . |
|
#5
|
|||
|
|||
|
ثالثاً : أشعاع بيتا الموجــ(β)ـــبة ( e + ) : - تعريفه : هو عبارة عن جسيمات ( شحنات ) موجبة تسمى البوزيترونات حيث أن البوزيترون هو جسيم له كتلة الإلكترون وشحنة البروتون . - صفات جسيمات بيتا الموجبة : نفس صفات جسيمات بيتا السالبة إلا أنها تعاكسها في الاتجاه عند دخولها عبر المجالين الكهربائي والمغناطيسي . - كيفية إنتاج جسيمات بيتا الموجبة : تتولد في النويات غير المستقرة والتي تكون فيها نسبة البروتونات أكبر من النيوترونات لذلك يتحول البروتون إلى نيوترون وبوزيترون . - المعادلة الأساسية لها : 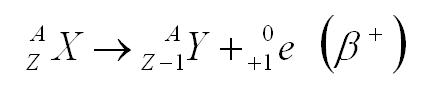 [flash=http://www.phys4arab.net/uploood/naser/nuclear04.swf]WIDTH=500 HEIGHT=100[/flash] http://www.phys4arab.net/uploood/naser/nuclear04.swf [flash=http://www.phys4arab.net/uploood/naser/nuclear11.swf]WIDTH=500 HEIGHT=400[/flash] http://www.phys4arab.net/uploood/naser/nuclear11.swf - مثال : النيتروجين 14 . - التغير الحاصل في الذرة عند إصدار جسيم بيتا الموجب : 1) ينقص العدد الذري وحدة ( أي ينقص بروتون واحد ) والعدد الكتلي ثابت . 2) يتحول العنصر إلى عنصر آخر . علل : تنحرف جسيمات ألفا بواسطة المجالين الكهربائي والمغناطيسي أقل من انحراف جسيمات بيتا ؟ ج / لأن كتلة جسيمات ألفا كبيرة ( جسيم موجب الشحنة ) بعكس جسيمات بيتا لذلك فهي تحتاج إلى طاقة أكبر لانحرافها . |
|
#6
|
|||
|
|||
|
رابعاً : الالتقاط الإلكتروني ( الأسر الإلكتروني ) : - تعريفه : هو قيام النواة بإلتقاط ( أسر ) إلكترون من مجال داخلي للذرة حيث ينتقل الإلكترون من المستوى الخارجي للطاقة إلى المستوى الداخلي للذرة فيتحد هذا الإلكترون مع بروتون ويتحول هذا البروتون إلى نيوترون مع إشعاع سيني . - المعادلة الأساسية له : 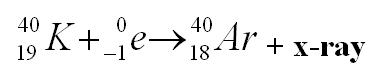 [flash=http://www.phys4arab.net/uploood/naser/nuclear05.swf]WIDTH=500 HEIGHT=100[/flash] http://www.phys4arab.net/uploood/naser/nuclear05.swf - مثال : البوتاسيوم 40 . - التغير الحاصل في الذرة عند الإلتقاط الإلكتروني ( إطلاق أشعة x ) : 1) العدد الذري ينقص وحدة ( أي ينقص بروتون واحد ) والعدد الكتلي ثابت . 2) يتحول العنصر إلى عنصر آخر . 3) تطلق أشعة سينية ( أشعة x ) . |
|
#7
|
|||
|
|||
|
خامساً : أشعة جاما ( γ ) :- تعريفها : هي عبارة عن أمواج كهرومغناطيسية تسير بسرعة الضوء وطاقتها عالية لا تتأثر بالمجالين الكهربائي والمغناطيسي . - صفات أشعة جاما : 1) ترددها عالي وطولها الموجي قصير . 2) طاقتها عالية . 3) لا تأين الذرات . 4) نفاذيتها عالية ( أكبر من جسيمات ألفا وبيتا ) حيث تستطيع اختراق جدار من الخرسانة سمكه 10 سم . علل : أشعة جاما لا تؤين ذرات الهواء بالرغم من ترددها العالي ؟ ج / لأن تردد هذه الأشعة عالي فإن طاقتها ستكون أكبر بكثير من طاقة الربط وبالتالي فهي مثل الموجه فوق السمعية التي لا تتأثر بها الأذن . - كيفية إنتاج أشعة جاما : تنتج من الذرات المثارة وسوف نضع الرمز ( * ) أعلى رمز العنصر من اليمين كدلالة على أن ذرة ذلك العنصر في حالة خاصة من الطاقة ( إثارة ) . - المعادلة الأساسية لها : 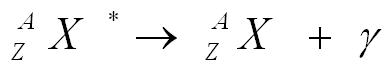 [flash=http://www.phys4arab.net/uploood/naser/nuclear10.swf]WIDTH=500 HEIGHT=400[/flash] http://www.phys4arab.net/uploood/naser/nuclear10.swf [flash=http://www.phys4arab.net/uploood/naser/nuclear13.swf]WIDTH=500 HEIGHT=400[/flash] http://www.phys4arab.net/uploood/naser/nuclear13.swf - مثال :التكتينيوم 99 المثارة ( انظر المعادلة ص 156 ) . - التغير الحاصل في الذرة عند إصدار أشعة جاما : لا يحدث أي تغير في الذرة ( أي لا تتحول نواة العنصر إلى عنصر آخر ) . علل : لا تتحول نواة العنصر إلى عنصر آخر عند إصدار أشعة جاما ؟ ج /لأنها أشعة عديمة الشحنة وكذلك العدد الذري والكتلي للذرة ثابتان لا يتغيران عند إصدارها . |
|
#8
|
|||
|
|||
|
نفاذية الجسيمات وأنحرافها في المجال المغناطيسي : [flash=http://www.phys4arab.net/uploood/naser/nuclear07.swf]WIDTH=500 HEIGHT=400[/flash] http://www.phys4arab.net/uploood/naser/nuclear07.swf [flash=http://www.phys4arab.net/uploood/naser/nuclear08.swf]WIDTH=500 HEIGHT=400[/flash] http://www.phys4arab.net/uploood/naser/nuclear08.swf [flash=http://www.phys4arab.net/uploood/naser/nuclear09.swf]WIDTH=500 HEIGHT=400[/flash] http://www.phys4arab.net/uploood/naser/nuclear09.swf [flash=http://www.phys4arab.net/uploood/naser/nuclear14.swf]WIDTH=500 HEIGHT=400[/flash] http://www.phys4arab.net/uploood/naser/nuclear14.swf [flash=http://www.phys4arab.net/uploood/naser/nuclear15.swf]WIDTH=500 HEIGHT=400[/flash] http://www.phys4arab.net/uploood/naser/nuclear15.swf [flash=http://www.phys4arab.net/uploood/naser/nuclear16.swf]WIDTH=500 HEIGHT=400[/flash] http://www.phys4arab.net/uploood/naser/nuclear16.swf [flash=http://www.phys4arab.net/uploood/naser/nuclear17.swf]WIDTH=500 HEIGHT=400[/flash] http://www.phys4arab.net/uploood/naser/nuclear17.swf أمثلة على الأشعاعات النووية : [flash=http://www.phys4arab.net/uploood/naser/nuclear06.swf]WIDTH=500 HEIGHT=400[/flash] http://www.phys4arab.net/uploood/naser/nuclear06.swf |
|
#9
|
|||
|
|||
|
اكتشاف النيوترون : إن اكتشاف النيوترون غير مفاهيم العلماء حول تركيب النواة , حيث كان يعتقد أن نواة الذرة تحتوي على عدد من البروتونات كتلتها تساوي الكتلة الذرية للعنصر , وعدد كاف من الإلكترونات لتحيط بها وتعادل شحنتها شحنة البروتونات , إلا أن مطياف الكتلة وضع أكثر من علامة استفهام حول ذلك الاعتقاد , حيث لاحظ العلماء أن مقدار الكتلة الذي يسجله مطياف الكتلة لأنوية العناصر يصل إلى ضعف كتلة هذه الأنوية ( أو أكثر ) التي نحصل عليه بطريقة حسابية ( على أساس أن كتلة مكونات النواة حسابيا = كتلة البروتون الواحد × العدد الذري للعنصر ) ولثقتهم بدقة حساباتهم وكذلك بدقة مطياف الكتلة فقد افترض العلماء وجود جسيمات متعادلة داخل النواة , بالإضافة إلى البروتونات.وتمكن بعد ذلك شادويك من إثبات وجودها عمليا . شادويك أجرى تجربته عام (1932م) واكتشف من خلالها النيوترون ومنح على ذلك جائزة نوبل . وتتلخص تجربة شادويك أنه قام بقذف هدف من البيريليوم بجسيمات ألفا (α) ونتج عن ذلك جسيمات لها قدرة نفاذ عالية , إذا سلطت هذه الجسيمات بحيث تسقط على لوح من البرافين فإنها تسبب في جعله يطلق بروتونات بسرعة عالية , واستطاع شادويك أن يثبت أن الجسيمات المنطلقة من البيريليوم هي عبارة عن جسيمات غير مشحونة ( لا تتأثر بالمجال الكهربائي أو المغناطيسي ) , كتلتها تساوي كتلة البروتون تقريبا سماها النيوترونات . [flash=http://www.phys4arab.net/uploood/naser/nuclear18.swf]WIDTH=500 HEIGHT=400[/flash] http://www.phys4arab.net/uploood/naser/nuclear18.swf وحيث أن النيوترون جسيم غير مشحون ( متعادل كهربائيا ) فهو يستخدم كقذيفة ممتازة لتحطيم النواة لأنه لا يتنافر معها , ولهذا السبب أيضا فإنه لا يسبب تأين المادة التي ينفذ من خلالها . وجدير بالذكر أن استخدام لوح البرافين في تجربة شادويك كان لتبطئة سرعة النيوترونات المتحررة , حيث تم تصادم النيوترون بذرة الهيدروجين (بروتون) المساوية له في الكتلة فيسكن النيوترون ويتحرر البروتون ( تصادم مرن بين جسمين متساويين في الكتلة أحدهما ساكن ) . |
|
#10
|
|||
|
|||
|
النشاط الأشعاعي Radioactivity مقدمة تاريخية : في عام 1896 م اكتشف هنري بكريل أن أحد أملاح اليورانيوم يصدر إشعاعا ، وذلك عندما وضع بكريل لوحا فوتوغرافيا مع معدن اليورانيوم في خزانة مظلمة وترك الفلم الفوتوغرافي مدة أربعة أيام, وبعد أن قام بتحميض الفلم لاحظ تكون صورة على الفلم الفوتوغرافي ، استنتج من ذلك أن معدن اليورانيوم قام بإطلاق أشعة غير مرئية أثرت على اللوح الفوتوغرافي . لم تكن طبيعة هذا الإشعاع واضحة في ذلك الوقت ، ثم اثبت بكريل أن الإشعاع الذي اكتشفه يصدر عن جميع مركبات اليورانيوم وعن اليورانيوم الفلزي أيضا بما يعني أن مصدر الإشعاع هو ذرة اليورانيوم واتضح له أن هذا الإشعاع يحدث بصورة تلقائية مستمرة لا تؤثر عليه المؤثرات الخارجية من ضغط ودرجة حرارة ولهذا سمى إشعاع اليورانيوم إشعاعا نشطا Radioactive Radiation وتسمى هذه الظاهرة النشاطية الإشعاعية Radioactivity . في عام 1898 م قام بكريل وزوجته مدام ماري كوري باكتشاف النشاط الإشعاعي للثوريوم وأيضا اكتشفا في نفس السنة عنصرين جديدين يوجدان في خامات اليورانيوم العنصر الأول أطلق عليه الراديوم وهو عنصر أقوى في نشاطه الإشعاعي من اليورانيوم بمليون مرة بينما العنصر الثاني أطلقا عليه اسم مسقط رأس م كوري وهو بولونيوم . وبعد 10 سنوات اكتشف رذرفورد في عام 1908 م الغاز النشط إشعاعيا -الرادون- بواسطة التحليل الطيفي. ودرس رذرفورد كذلك طبيعة النشاط الإشعاعي لبعض العناصر فتبين أن العناصر المشعة تعطي ثلاثة أنواع من الأشعة والدقائق والتي تعرف حاليا بأول ثلاثة حروف من الأبجدية الإغريقية وهي ألفا, بيتا, جاما . واليوم تعرف دقائق ألفا بأنها نواة ذرة الهيليوم والمكونة من بروتونين ونيوترونين, وتعرف دقائق بيتا على أنها الكترونات ذات طاقة عالية, وتعرف أشعة جاما بأنها أشعة كهرومغناطيسية. سميت ظاهرة إطلاق بعض العناصر للأشعة بظاهرة النشاط الإشعاعي.. تعرف اليوم ظاهرة النشاط الإشعاعي على أنها ظاهرة الانبعاث التلقائي للدقائق أو الطاقة من انويه الذرات. تفسير النشاط الأشعاعي : بعض المواد (العناصر) الموجودة في الطبيعة تكون غير مستقرة، الأمر الذي يحملها على القيام ببعض العمليات بحثاً عن الاستقرار. هذه العمليات (التلقائية) هي عبارة عن إضمحلالات للأنوية والتي قد تترك النواة الناتجة في حالة إثارة مما يؤدي إلى انبعاث أشعة نووية. وبهذا تعتبر هذه المواد مواداً مشعة أو نشطة إشعاعياً ويمكن أن تعتبر مصادر إشعاعية. [flash=http://www.phys4arab.net/uploood/naser/nuclear19.swf]WIDTH=500 HEIGHT=400[/flash] http://www.phys4arab.net/uploood/naser/nuclear19.swf [flash=http://www.phys4arab.net/uploood/naser/nuclear22.swf]WIDTH=500 HEIGHT=400[/flash] http://www.phys4arab.net/uploood/naser/nuclear22.swf النشاط الإشعاعي الطبيعي في القشرة الأرضية: عُرفت أهم العناصر المشعة في صخور القشرة الأرضية في ثلاث سلاسل وهي : ( اليورانيوم -238 ) و( اليورانيوم -235 ) و( الثوريوم -232 ) ، ويوجد على رأس كل سلسلة نظير طويل العمر في حين تنتهي كل منها بنظير مستقر للرصاص, فسلسلة ( اليورانيوم – 238 ) على سبيل المثال, الناتج النهائي للانحلال هو ذرة الرصاص المستقر. 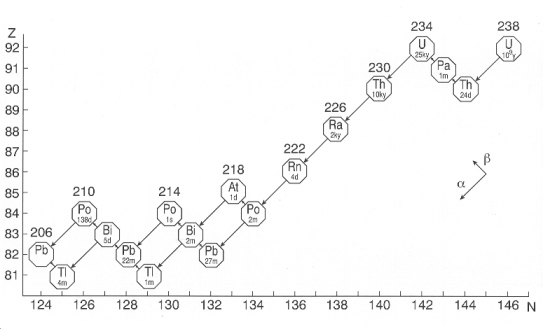 وهناك ما يقارب الأربعين من النظائر المشعة . وأعمار النصف للعناصر المشعة الأساسية في صخور القشرة الأرضية طويلة جداً ، لهذا بقيت في الأرض إلى الآن منذ خلقها ، فعمر النصف ( للبوتاسيوم -40 ) يزيد على ألف مليون سنة وعمر النصف ( الروبيدوم -87) يزيد على أربعين ألف مليون سنة . مثال : نظير الراديوم - 226 - يتحلل إلى الرادون - 224 الذي يتحلل بدوره إلى البولونيوم - 218 الذي يتحلل إلى الاستاتين -218 ، وهكذا تستمر السلسلة حتى تتوقف عند عنصر الرصاص المستقر (206) . فيديو النشاط الأشعاعي لـ ( الراديوم والكربون و البلوتونيوم ) http://www.phys4arab.net/uploood/nas...ioactivity.rar 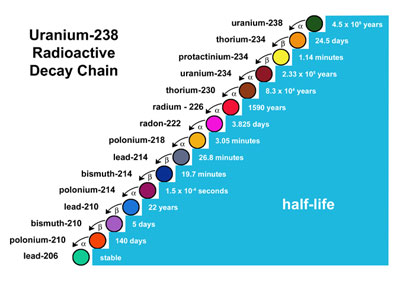 ومستوى النشاط الإشعاعي الطبيعي في القشرة الأرضية متقارب جداً في معظم الأماكن ، حيث لا يوجد اختلاف يذكر عن مكان وآخر بصفة عامة . إلا أن هناك أماكن على الأرض يزداد فيها الإشعاع الطبيعي بشكل كبير نتيجة وجود تركيزات عالية من العناصر المشعة طبيعياً في صخور القشرة الأرضية . 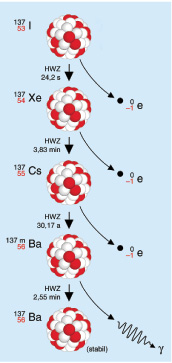 النشاط الإشعاعي الصناعي: ولقد اجتهد الإنسان في تطور العلوم بفروعه المختلفة بما فيها الفيزياء إلى أن تمَّ التوصل إلى اكتشاف الإشعاع الصناعي وذلك باكتشاف الأشعة السينية X ray عام 1895م على يد رونتجن. وتوالت بعد ذلك الاجتهادات والاكتشافات الفيزيائية والإشعاعية من قِبَلِ كلٍّ من رذرفورد و السيدة ماريا كوري وزوجها بكريل إلى أن أصبح الإشعاع من أهمَّ الظَواهر التي يتحدث عنها الناس ومن الأمور التي لا غِنى عنها في حياتنا المعاصرة وأصبحت الحاجة إليه تزداد بصورة تصاعدية ، وقد اتسع نطاق استعمال النظائر المشعة في العديد من مجالات الحياة الطبية والزراعية والصناعية, ويمكن إيجاز بعض هذه الاستعمالات: [flash=http://www.phys4arab.net/uploood/naser/nuclear21.swf]WIDTH=500 HEIGHT=400[/flash] http://www.phys4arab.net/uploood/naser/nuclear21.swf فقد استخدمت النظائر في علاج السرطان حيث تخترق أشعة جاما الأنسجة وتقتل الخلايا الحية, ولذلك يسلط على الأورام السرطانية شعاع عالي التركيز من مصدر للكوبالت - 60 والذي يعمل على قتل الخلايا السرطانية في الورم, وقد استخدم نظير الفسفور المشع في علاج سرطان الدم, وذلك بإعطاء المريض جرعات خاصة تحتوي على نظير الفسفور المشع, حيث يحد من إنتاج كرات الدم الحمراء. اما من حيث المجال الزراعي فقد تمكن العلماء الايطاليون من إنضاج القمح في مدة لا تتجاوز 64 يوما, بينما هو في الحالة الطبيعية ينضج في 7 أشهر, وقد استخدم إشعاع الكوبالت في تغيير لون البلاستيدات الملونة, وذلك بتعريض النبات لفترات مختلفة للإشعاع, مما يتيح وجود أزهار بألوان مختلفة على النبات نفسه, وقد استخدم إشعاع الكوبالت المسلط على طعام الماشية لزيادة السمنة فيها وزيادة إدرارها اللبن. [flash=http://www.phys4arab.net/uploood/naser/nuclear20.swf]WIDTH=500 HEIGHT=400[/flash] http://www.phys4arab.net/uploood/naser/nuclear20.swf خطر النشاط الإشعاعي: ومما لا يدركه البعض أننا قد نتعرض للإشعاع خصوصاً المؤين منه من بيئتنا التي نعيش فيها وذلك عن طريق الهواء الذي نستنشقه أو الماء الذي نشربه والطعام الذي نأكله. حيث يوجد البعض من العناصر المشعة مثل البوتاسيوم Potassium) K) والرادون Radon) Rn) والراديوم Radium) Ra) إلى ما غير ذلك من المصادر التي ربما كان للإنسان سبباً في وجودها. وعلى هذا فيمكننا تقسيم الإشعاع المؤين إلى قسمين، إشعاعات طبيعية وإشعاعات صناعية. وقد أصبح لهذه الإشعاعات (النووية والذرية) تطبيقات واسعة في مجالات عديدة منها الصناعي مثل صناعة الأسلحة وحفظ الأغذية، ومنها الطبي بفرعيه التشخيصي والعلاجي ومنها الزراعي حيث تحسين المحاصيل الزراعية. وجميع هذه التطبيقات تعتمد على تفاعلات الأشعة المؤينة التي تحدث في المادة. والكائن الحي معرض للمجال الإشعاعي المؤين عن طريق المصادر الإشعاعية خصوصاً الطبيعي منها وبالتالي سيتعرض لجرعات إشعاعية دون الشعور بذلك ولذا وجب معرفة كمية الإشعاع المؤين وذلك عن طريق قياس وتحديد هذه الجرعات باستخدام الأجهزة والكواشف الإشعاعية الخاصة بذلك. وعلى الرغم من انتشار استخدام الأشعة المؤينة إلا أن لها أضراراً بالغة في الخطورة منها الداخلي ومنها الخارجي وقد يتطور الضرر الإشعاعي ويؤدي إلى استثارة الخلايا السليمة وتحولها إلى خلايا سرطانية أو ربما أدى إلى موتها وتلفها. الخلاصة: تعريف النشاط الإشعاعي: يُعَرَّفْ النشاط الإشعاعي بأنه عدد النوى المنحلة من هذا العنصر في الثانية الواحدة. و يُعَرَّفْ أيضا بأنه : عملية تلقائية يتحول فيها العنصر إلى عنصر آخر نتيجة فقد جسيمات ألفا أو جسيمات بيتا أوانطلاق أشعة جاما . ملاحظات : 1) العنصر المشع جميع مركباته مشعة . 2) العنصر المشع يكون مشعاً في جميع حالاته (صلبة – سائلة – غازية) . 3) نواة العنصر المشع لا تصدر جسيمات ألفا وجسيمات بيتا معاً ، ولكن قد تصدر ألفا أو بيتا ، وقد يصاحب كلاً منهما انطلاق إشعاعات جاما . 4) معدّل النشاط الإشعاعي لعينة مشعة لا يتأثر بالظروف الخارجية من ضغط أو درجة حرارة ولكنه يتوقف فقط على نسبة العنصر المشع في العينة . 5) انبعاث جسيم بيتا أو جسيم ألفا من نواة العنصر المشع يحولّها إلى نواة عنصر آخر . الفرق بين النشاط الإشعاعي والتحول الكيميائي: يختلف النشاط الإشعاعي عن التحول الكيميائي في 1- النشاط الإشعاعي عملية تلقائية مستمرة 2- يعتمد على العنصر المشع ولا يرتبط بالمركب الكيميائي 3- لا يتوقف على الظروف الفيزيائية ( الضغط ، درجة الحرارة ) 4- تنطلق منه طاقة هائلة استنتج قانون الانحلال الإشعاعي: . تعتبر ظاهر النشاط الإشعاعي ظاهرة إحصائية ، أي أنه لا يمكن التكهن بزمن تنحل عند نواة بعينها ، ولكن عند وجود عدد كبير جداً من أنوية النظير المشع ، فإنه بمتابعة معدل تغير كمية الأشعة المنبعثة يمكن معرفة الكثير عن نوعية التحول . هناك احتمال محدد للنشاط في وحدة الزمن لأي نظير مشع ، وهذا الاحتمال يعرف بثابت مميز لكل نظير مشع بغض النظر عن حالته . الكيميائية أو الفيزيائية ( من سائله أو صلبه أو غازية ) . فإذا كان ( ن ) عدد الأنوية المشعة الموجودة في عينة ما عند زمن ( ز ) فإن معدل النشاط يعطي المعادلة - دالتا ( ن ) /دالتا ( ز ) = ل × ن حيث تسمى ( ل ) بثابت الانحلال ( decay Constant ) وهو يعد مقياساً لاحتمال انحلال نواة معينة ، و " الإشارة السالبة أن تعني أن عدد النويات يتناقض مع الزمن " - دالتا ( ن ) /دالتا ( ز ) تعني التغير في عدد الذرات (الأنوية) بالنسبة للزمن الذي حدث فيه التغير , وهو مايسمى النشاطية الإشعاعية , وتقاس بوحدة ( انحلال / ثانية ) وهناك وحدة أخرى هي (كوري) . حيث 1 كوري = 3.7 × 10 ^10 انحلال / ثانية . وباجراء عملية التكامل لطرفي المعادلة السابقة نحصل على علاقة يمكن من خلالها معرفة عدد نويات العنصر أو ( كتلة العنصر ) المتبقية بعد مضي زمن قدره (ز) , وهذه العلاقة هي : ن = ن0 × و ^ ( – ل × ز ) أو ك = ك0 × و ^ ( – ل × ز ) وحدة قياس النشاطي الإشعاعي تقاس النشاطية الإشعاعية بوحدة البكريل البكريل البكريل هو عدد الإشعاعات التي تصدرها العينة المشعة في الثانية ما معنى أن النشاطية الإشعاعية لعينة واحد بكريل ؟ المعنى : نشاطية العينة تصدر إشعاعا واحدا في الثانية وحدات أخرى لقياس النشاطية الإشعاعية نعم توجد وحدة انحلال / ثانية ، وحدة الكوري Ci وفي بعض المراجع Cu وأيضا توجد وحدة ثالثة هي الرذرفورد Rd وهو نشاط يناظر مليون انحلال / ثانية الكوري الكوري هو نشاط عينة تنحل فيها في الثانية الواحدة 3.7x1010 من الانوية المشعة |
«
الموضوع السابق
|
الموضوع التالي
»
| الذين يشاهدون محتوى الموضوع الآن : 1 ( الأعضاء 0 والزوار 1) | |
| أدوات الموضوع | |
| انواع عرض الموضوع | |
|
|
المواضيع والمشاركات المنشورة لا تعبر عن رأي ملتقى الفيزيائيين العرب ولانتحمل أي مسؤولية قانونية حيال ذلك ويتحمل كاتبها مسؤولية النشر"
الساعة الآن 05:30






 العرض العادي
العرض العادي

